Team « Metaorganisms » – Pre Yasmine Belkaid
Elle explore les mécanismes fondamentaux qui régulent l’homéostasie tissulaire et les réponses immunitaires de l’hôte. Elle a ainsi mis en évidence les rôles clés du microbiote et des facteurs alimentaires dans le contrôle de l’immunité et la protection contre les agents pathogènes. Elle étudie également le rôle du système immunitaire dans le remodelage de l’organisme et l’impact des infections sur la dyade mère-enfant.
Team « Macrophages and endothelium » – Dre Elisa Gomez Perdiguero
Nous étudions comment l’embryon génère la diversité des cellules sanguines et immunitaires (globules rouges, plaquettes, lymphocytes, macrophages), un processus complexe et temporellement régulé. Comprendre cette « chorégraphie cellulaire » est essentiel pour expliquer les troubles hématologiques pédiatriques, souvent différents de ceux de l’adulte : certains se résolvent spontanément, tandis que d’autres, comme les hémoglobinopathies, restent asymptomatiques à la naissance.
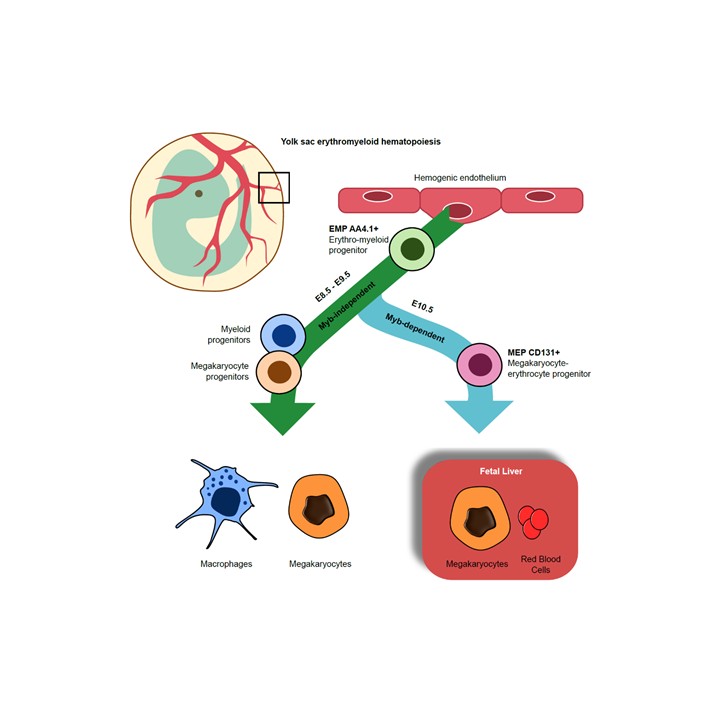
Les chercheurs s’intéressent particulièrement aux progéniteurs érythroïdes/myéloïdes (EMP), issus de l’endothélium hémogénique du sac vitellin, premier site de production sanguine embryonnaire. Longtemps considérés comme transitoires, les EMP révèlent une dynamique plus complexe que prévu. Leur étude, publiée dans Immunity, montre que les EMP passent par deux phases de différenciation : d’abord dans le sac vitellin, où ils forment rapidement macrophages et mégacaryocytes ; ensuite, plus tard, en migrant vers le foie fœtal pour produire une variété de cellules (érythrocytes, monocytes, granulocytes, mastocytes).
Les mégacaryocytes, sources des plaquettes, proviennent de deux voies distinctes impliquant les EMP. Leur production précoce est cruciale pour la coagulation, l’hémostase et la séparation des systèmes sanguin et lymphatique. Ces travaux révèlent une hétérogénéité inattendue des EMP et une différenciation plus complexe que celle décrite précédemment, ouvrant de nouvelles perspectives pour la compréhension des maladies du sang chez l’enfant.
Team « Microenvironment and immunity » – Pr Gérard Eberl
Le système immunitaire, le système nerveux et les microbes symbiotiques interagissent à de nombreux niveaux pour faire face aux menaces pesant sur l’individu et maintenir l’homéostasie.
Le microbiote intestinal joue un rôle central dans le développement et la régulation du système immunitaire, notamment en stimulant la formation de tissus lymphoïdes dans l’intestin après la naissance. Les bactéries libèrent des muropeptides, détectés par le récepteur Nod1 des cellules épithéliales, ce qui active des cellules immunitaires (comme les LTi et les lymphocytes B IgA+), régulant ainsi le microbiote pour éviter les déséquilibres.
Le microbiote influence aussi la différenciation de cellules immunitaires (ILC, Th17, iTreg). Son altération peut entraîner des maladies inflammatoires chroniques, allergies ou auto-immunes. Pendant le sevrage, une « réaction de sevrage » se produit, marquant durablement la réactivité immunitaire (empreinte néonatale). Une perturbation de cette phase augmente le risque de pathologies inflammatoires à l’âge adulte.
Le système nerveux et le système immunitaire partagent des mécanismes de détection et de mémoire pour répondre aux menaces (antigènes, lésions, température, etc.). Ils agissent de manière complémentaire, notamment lors de l’ingestion d’aliments, où des neuropeptides renforcent l’action des cellules immunitaires intestinales contre les pathogènes.
Enfin, le microbiote communique directement avec le système nerveux central : les muropeptides bactériens atteignent l’hypothalamus, modulant l’appétit et la température corporelle. Des souris sans récepteur Nod2 développent obésité et troubles thermiques. Le stress chronique altère aussi le microbiote, réduisant la production de tryptophane et d’autres métabolites, favorisant des symptômes dépressifs transmissibles à un nouvel hôte.
En résumé, ces trois systèmes s’influencent mutuellement pour assurer la santé et la survie de l’individu
National Reference Center Listéria – Pr Marc Lecuit
L’unité de Biologie des Infections (Institut Pasteur, Inserm) s’intéresse à la compréhension des mécanismes infectieux, tant du point de vue de l’hôte que du pathogène. Elle se concentre plus particulièrement sur les infections invasives touchant le système nerveux central, ainsi que sur les infections materno-fœtales et néonatales. Dans ce contexte, nous étudions le pathogène modèle Listeria monocytogenes, responsable d’infections materno-fœtales pouvant conduire à des fausses couches, des avortements, des accouchements prématurés, ainsi que des infections fœtales et néonatales systémiques et neurologiques. Grâce au Centre National de Référence et Centre Collaborateur de l’OMS Listeria, qui est associé à notre laboratoire, nous combinons des études épidémiologiques, cliniques, microbiologiques, immunologiques, cellulaires, génétiques et physiopathologiques humaines et expérimentales, menées selon une approche multidisciplinaire et intégrative, afin de comprendre les mécanismes de l’infection maternelle, placentaire et fœtale et ses conséquences immédiates et à long terme chez la mère et l’enfant. L’expertise que nous avons développée est également mise à profit pour l’étude des infections liées aux virus émergents qui présentent un tropisme similaire à Listeria monocytogenes. Dans ce cadre, notre laboratoire a contribué à la compréhension des infections liées aux virus chikungunya et Zika, à l’entérovirus 71 et au Sars-CoV-2.
